膠質母細胞瘤(GBM)是最具侵襲性原發性腦腫瘤(之一),具有死亡率高、生存期短、預後差、複發率高的特點。在過去的幾十年裏,針對膠質母細胞瘤(GBM)的治療效果幾乎沒有取得什麼突破性進展,患者5年生存率僅為5%左右。
在膠質母細胞瘤的治療中,手術和化療藥物的治療效果主要受到精細腦結構、血腦屏障(BBB)或血腦腫瘤屏障(BBTB)的阻礙。特別是,將治療腦腫瘤的藥物給藥到中樞神經係統(CNS)非常具有挑戰性。已發表的數百項研究顯示,給藥的納米顆粒劑量被遞送到實體瘤的比例不足1%,而被遞送到腦腫瘤中的不足0.8%。
中性粒細胞(Neutrophils)具有向炎症部位遷移、穿越血腦屏障/血腦腫瘤屏障和浸潤實體瘤的天然能力,因此可用於增強對腦腫瘤的靶向藥物遞送,以提高治療效果。然而,在中性粒細胞/化療給藥之前,需要侵入性手術切除腫瘤或腫瘤微環境啟動來誘導中性粒細胞募集的額外炎症,這導致炎性手術邊緣以外腫瘤部位的中性粒細胞募集有限。此外,中性粒細胞遞送的化療藥物主要富集於脾髒,而不富集於腦腫瘤部位。中性粒細胞壽命短且易在體外凋亡,在患者術前大量提取中性粒細胞用於藥物遞送可能導致其中性粒細胞減少,這些障礙是的使用人類中性粒細胞進行藥物遞送的可行性及安全性難以捉摸。因此,迫切需要一種安全有效的人中性粒細胞介導的仿生給藥係統。
2023年4月20日,普渡大學包小平團隊等在 Nature 子刊 Nature Communications 上發表了題為:CAR-neutrophil mediated delivery of tumor-microenvironment responsive nanodrugs for glioblastoma chemo-immunotherapy 的研究論文。
研究團隊使用CRISPR-Cas9介導的基因敲入對人類多能幹細胞(hPSC)進行基因工程改造,以表達具有T細胞特異性CD3ζ或中性粒細胞特異性γ信號域的各種抗膠質母細胞瘤CAR結構,從而構建出具有最佳抗腫瘤活性的CAR-中性粒細胞(CAR-NE),其能夠特異性且無創地遞送和釋放腫瘤微環境響應的納米藥物,以靶向膠質母細胞瘤,而無需在腫瘤部位誘導額外的炎症。
這種化學免疫聯合療法在腫瘤小鼠模型中表現出優越的特異性抗膠質母細胞瘤活性,減少藥物脫靶遞送並延長了腫瘤小鼠壽命。
總的來說,該研究開發的仿生CAR-中性粒細胞給藥係統是一種安全、有效和通用的藥物遞送平台,為膠質母細胞瘤等毀滅性疾病帶來了新的潛在治療手段。

嵌合抗原受體(CAR)修飾的T細胞(CAR-T)或自然殺傷細胞(CAR-NK)具有顯著的抗腫瘤活性,但它們在實體瘤中的療效仍然有限,部分原因是它們相對較低的遞送和腫瘤穿透能力。生理性血腦屏障(BBB)和血腦腫瘤屏障(BBTB)的存在進一步阻礙了這些新興細胞療法對膠質母細胞瘤(GBM)的療效。
中性粒細胞對各種癌症具有先天免疫和可塑性,但其作為藥物遞送細胞載體的應用研究較少。在這項研究中,包小平團隊等認為CAR-中性粒細胞(CAR-NE)可能在膠質母細胞瘤的治療中產生良好的效果。
原代中性粒細胞壽命較短,對基因組編輯具有抗性,這限製了它們在CAR修飾的免疫治療中的應用。人類多能幹細胞(hPSC)更容易進行基因組編輯,然後再大量分化為中性粒細胞,從而為免疫治療提供大量的高質量CAR-中性粒細胞來源。
在這項工作中,研究團隊設計和篩選了四種具有T細胞或中性粒細胞特異性信號域的抗膠質母細胞瘤的氯離子通道毒素(CLTX)-CAR結構,通過CRISPR-Cas9介導的同源重組將它們敲入hPSC的AAVS1安全港位點,並鑒定了一種優化的CAR,其由36個氨基酸的膠質母細胞瘤靶向CLTX肽,CD4跨膜結構域和CD3ζ胞內結構域組成,用於中性粒細胞介導的腫瘤殺傷。
由此產生的穩定表達CAR的hPSC分化為CAR-中性粒細胞,其維持了抗腫瘤N1表型,並在缺氧腫瘤微環境下表現出增強的抗膠質母細胞瘤活性。
接下來,研究團隊合成了一種具有粗糙表麵的可生物降解介孔有機二氧化矽納米顆粒(R-SiO2),並用於將化療藥物替拉紮明(TPZ)或替莫唑胺(TMZ)和JNJ-64619187裝載到hPSC分化而來的CAR-中性粒細胞中,這些中性粒細胞不受納米負載的傷害,並保留幼稚中性粒細胞固有的生物生理特性。
CAR-中性粒細胞裝載含有化療藥物的SiO2納米顆粒,顯示出優越的抗膠質母細胞瘤活性,這可能是由於CAR增強的直接細胞溶解和化療介導的腫瘤殺傷的結合。

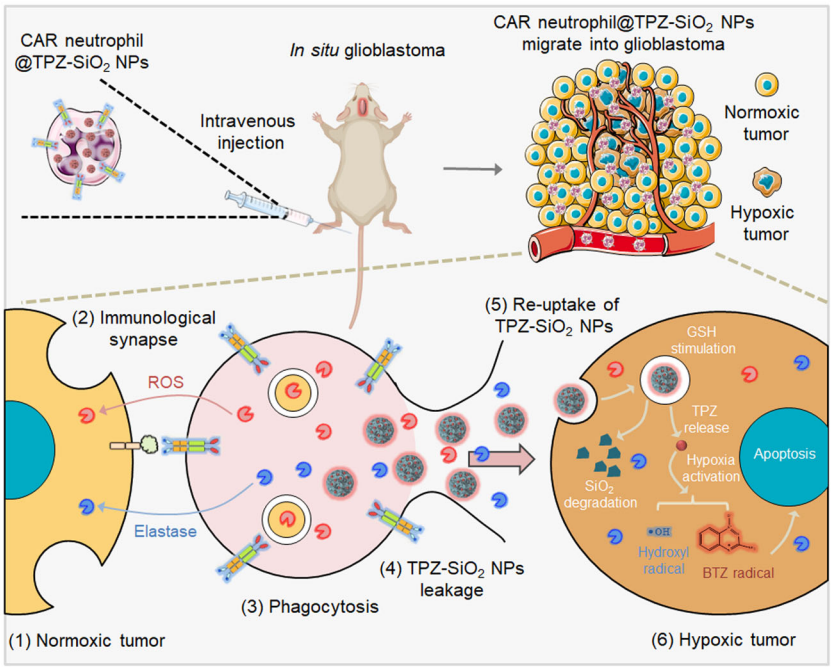
在原位膠質母細胞瘤異種移植模型中,hPSC分化而來的CAR-中性粒細胞精確有效地將負載替拉紮明(TPZ)的SiO2納米顆粒遞送到腦腫瘤中,而無需侵入性手術切除以擴大炎症,並顯著抑製了腦腫瘤生長,延長動物存活時間,這代表了一種靶向和有效的化學-免疫聯合治療。
值得注意的是,通過對矽含量的檢測表明,20%的納米藥物通過CAR-中性粒細胞遞送到了腦腫瘤中,這遠超常規納米藥物通過循環係統的不足1%的腦腫瘤遞送效率。
總的來說,這項研究開發了一種仿生CAR-中性粒細胞遞藥係統,並證明了其可作為一種安全、有效和通用的藥物遞送平台,可用於治療膠質母細胞瘤和其他毀滅性疾病。
原始出處:
Chang, Y., Cai, X., Syahirah, R. et al.CAR-neutrophil mediated delivery of tumor-microenvironment responsive nanodrugs for glioblastoma chemo-immunotherapy. Nat Commun 14, 2266 (2023). https://doi.org/10.1038/s41467-023-37872-4.