【概述】
腦膠質瘤病(Gliomatosis cerebri,GC)是一種原發性腦瘤,以神經膠質細胞彌漫性增生而原有大體解剖結構保持相對完整為特征;Nevin於1938年首次提出“腦膠質瘤病”的概念;1986年Troost等基於臨床症狀、影像學檢查及活檢病理,第一次於患者生前確診GC。由於GC惡性程度較高、臨床及影像學表現特異性不強,因此隻有在屍檢時才被確診。近年來隨著神經病理學和影像學的發展,臨床病例報告逐漸增多,但在病理活檢前對疾病做出診斷仍存較大難度。
病因及發病機製
GC的病因未明,其發病機製主要有三種假說:(1)神經膠質係統先天性發育不良,導致膠質細胞間變為瘤細胞並呈彌漫性浸潤性生長;(2)腫瘤起源於多個瘤細胞分化中心並呈彌散性浸潤生長;(3)腫瘤細胞呈灶內增殖擴散或區域性轉移擴散。關於瘤細胞起源,亦眾說紛紜;2007年WHO對中樞神經係統腫瘤分類時,將GC歸為神經上皮組織起源腫瘤中的星形膠質細胞腫瘤。
組織病理學表現
依大體形態將GC分為I型和II型;I型主要表現為彌漫性浸潤性生長,一般無明顯腫塊、結節、囊變等;II型較為少見,可能由I型發展而來,表現為在I型基礎上出現腫塊、結節、囊變等明顯密度變化區,具有高級別膠質瘤特點。腫瘤浸潤區一般表現為:腦組織輕微腫脹,灰質和白質及浸潤區和非浸潤區分界不清,主要累及腦白質,保留組織結構大體輪廓;鏡下可見各類分化程度不同的瘤細胞沿神經束及血管周圍浸潤性生長,呈橢圓形或梭形,多數體積小,胞質少,核形態多樣但少見分裂相。多數瘤細胞起源於星形膠質細胞,因此其超微結構類似於星形膠質細胞的超微結構;主要表現為核內染色質均勻分布,胞漿及胞突內含有多少不等的中間絲,缺少細胞連接,胞外無膠原及高電子密度的基質。
影像學表現
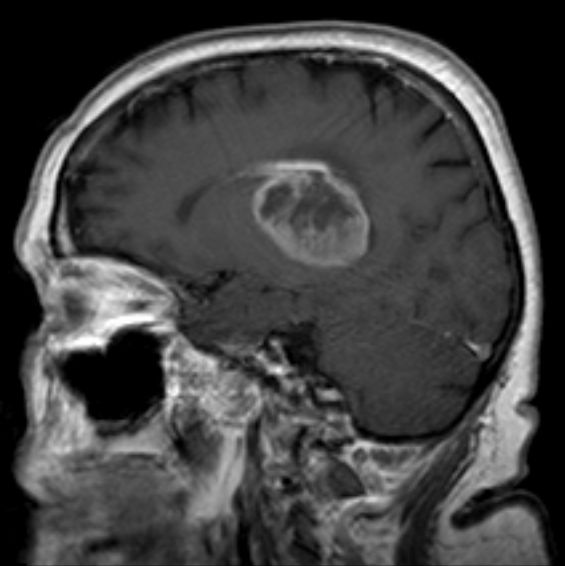
影像學檢查對GC的診斷有重要價值,CT表現為彌漫性等密度/低密度改變,缺乏特異性;MRI表現為以長T1、長T2為主的彌漫性信號改變,邊界不清,增強掃描:I型無明顯強化,II型表現為彌漫性病變區域內可見部分強化。由於MRI的獨特優勢,目前其已成為GC的首選影像學檢查;主要表現為瘤細胞廣泛浸潤和白質脫髓鞘改變,占位效應不明顯,少見結節、囊變等改變;累及兩個以上腦葉,甚至脊髓;胼胝體最常受累,表現為彌漫性腫脹,邊界模糊,Essig等認為此征象對診斷GC有重要價值;病變區在T1像上為低信號/等信號,在T2像及FLAIR像上為高信號/混雜高信號,其中T2像和FLAIR像可以清晰顯示病變範圍、形態;增強掃描多無強化,偶見部分強化,這表明血腦屏障遭到破壞,腫瘤侵及腦膜及血管,提示該區域惡性變。盡管MRI對GC的診斷有重要價值,但其顯示病變仍小於實際浸潤區。磁共振波譜(magnetic resonance spectroscopy,MRS)作為對GC的補充性檢查,能定量檢測腫瘤的能量代謝及生化改變,表現為NAA降低,Cho、Cho/Cr及Cho/NAA上升;有學者提出其對腫瘤分級、鑒別診斷、穿刺定位及療效評估具有極大價值。再結合動態對比增強磁共振成像(dynamic contrast-enhanced magneticresonance imaging,DCE-MRI)可以進一步提高顱內腫瘤的鑒別;DCE-MRI作為一種無創成像技術,其通過獲得容積轉運參數(Ktrans)和血管外細胞外間隙容積比(Ve)定量測量腫瘤不成熟微血管的通透性,從而評估腫瘤病理分級。Cai等研究還發現,PET與MRI相比,能更準確地反映GC的浸潤範圍及惡性程度。
臨床表現
研究表明,GC從新生兒至85歲老人均可發病,中年人居多,多數患者起病緩慢、隱匿,臨床表現複雜多樣,患病早期缺乏特征性表現;臨床症狀以不同程度精神和性格改變為主(78%),還可出現偏癱(59%)、共濟失調(50%)、癲癇(50%)、腦幹受累(50%)、視乳頭水腫(47%)、頭痛(41%)等;此外還有新生兒顱內出血、類似於蛛網膜下腔出血、合並內生軟骨瘤病及鈣化上皮瘤的報道。
【診斷和鑒別診】
臨床診斷
結合臨床、影像及病理方可對GC做出準確診斷;依據如下:(1)早期多有精神及性格改變;(2)不明原因的癲癇、偏癱、失語和共濟失調等臨床表現;(3)顱內壓增高,但腦脊液蛋白含量正常或輕度升高,細胞數多正常,偶見瘤細胞;(4)影像學顯示腦內彌漫性病變,中線居中或輕度偏移,腦室不同程度變窄,占位效應不明顯,少見結構明顯改變;(5)病理診斷明確。
鑒別診斷
GC應與下列疾病相鑒別:(1)多發性膠質瘤:兩個以上部位同時出現膠質瘤,病灶間無明顯聯係,出血壞死多見,可呈明顯強化。(2)惡性浸潤性膠質瘤:此類病變惡性度高,占位效應明顯,多有壞死、囊變,MRI信號不均勻,增強掃描呈不同形式強化。(3)脫髓鞘病變:特別是占位效應明顯的多發性硬化斑塊,常規MRI上難以與GC相鑒別,但MRS對疾病的鑒別診斷有重要價值;對激素治療效果也可鑒別;此外Park等發現腫瘤蛋白P53及腫瘤增殖核抗原Ki-67的測定也有助於鑒別。(4)腦內病毒性感染:從其臨床表現、實驗室檢查、抗感染治療效果及病程演變可對疾病做出診斷。
【治療和預後】
目前,國內外對GC的治療尚處於探索階段,關於疾病的治療尚存爭議,沒有共識;其治療手段主要包括手術、藥物療法、放射療法。
手術
由於病變範圍廣,難以全切,有學者不主張行手術治療;為了明確病理,可以在立體定向或神經導航引導下對顱內多發病灶進行活 檢術。另有學者則認為,術者應在最大可能保留神經及功能的原則下最大限度切除腫瘤,達到明確病理、緩解高顱壓、減少載瘤量、提高放化療療效的目的;對可疑惡性病變的結節行手術切除,可延緩病情,提高生存期;Pérez-Bovet等曾對一患者行顳葉切除術以降低高顱壓,後行放化療,延長患者生命23月;Chen等提出手術可以提高患者對放療的療效,從而改善生存質量、延長生存期。為降低功能區腫瘤的致殘率,功能磁共振已越來越多地應用於手術規劃,並取得了令人鼓舞的成果。總之,手術對GC治療效果有限,但其對於明確診斷、改善危急症狀、減少載瘤量具有不可替代的作用。
藥物療法
藥物療法作為惡性腫瘤治療的常規手段,臨床研究表明,早期化療對腫瘤的控製效果顯著。Levin等發現,PCV方案(甲基苄肼+羅氮 芥+長春新堿)和替莫唑胺對GC療效相當,可使患者的症狀改善率及影像學控製率分別達33%和26%;但替莫唑胺作為新一代烷化劑,能夠通過血腦屏障且優先聚集於腦腫瘤組織中,作用於瘤細胞分裂的各個時期,使其DNA烷基化,從而發揮細胞毒性作用;多個研究組對替莫唑胺的研究肯定了其抗腫瘤療效和低毒副作用,從而主張將其作為惡性膠質瘤化療的一線藥物;此外,還有研究發現,局部控釋化療的應用對控製局部病變及減少化療毒副作用效果顯著。目前,臨床上化療藥物種類繁多,僅憑經驗難以取得良好效果 ,Fang等認為,在體外組織塊培養藥敏試驗(tissue culture-end point staining-computer image analysis,TECIA)指導下製定個體化化療方案可以提高化療療效,臨床研究也證實對此方法有較好療效。因此,臨床中可以根據TECIA對GC患者實施個體化化療。
放射療法
2006年Taillibert等對296例GC患者回顧性分析後提出,放療與否對患者的生存期並無顯著影響;但是隨著放射治療設備和技術的飛速發展,其已成為國內外治療惡性膠質瘤的主要手段。Kim等報道15例GC患者經外放射治療後,其平均生存期為38.4月;Wang等還發現,放療相對於化療可以更快地降低高顱壓。目前,圖像引導放射治療及適形調強放射治療作為國外主流放療技術,已取得良好臨床效果;特別是適形調強放射技術,可以減少30%-50%的正常組織損傷,在盡量保護正常組織的同時增加腫瘤的照射劑量;目前,最新研發的容積弧形調強放射技術可以更加精準的對腫瘤實施個體化放療,其療效已在鼻咽癌、宮頸癌、直腸癌等多個惡性腫瘤的臨床應用中得到證實。未來,放射技術和設備的發展定會為GC的治療帶來突破性進展。
聯合療法
鑒於GC的特性,單一療法往往難以控製疾病進展。Kong等分析了37例GC病例發現,放化療較單純放療的平均生存期延長11.1月;Mattox等則通過對30例替莫唑胺或(和)全腦放療患者的臨床資料研究發現,患者平均生存期為25月,一年和兩年生存率達89%和55%;Inoue等回顧性分析了局部放療和靜脈注射尼莫司汀的病例,其中4例聯合替莫唑胺治療,患者一、三、五年生存率分別為70.6%、23.5%、17.7%;這與多個學者的研究結果一致,放化療聯合應用可以明顯延長生存期;近來,Kyritsis等通過分析近10年間有關高級別膠質瘤標準化治療方案(手術+放療+替莫唑胺)失敗後,針對腫瘤複發和進展的二線治療手段(福莫司汀、貝伐單抗等單藥或聯合方案)的臨床報道,發現治療效果並不理想。因此,對於GC的治療,應盡早明確診斷,必要時行病理活檢,然後根據患者病情及對化療藥物的敏感性行同步放化療。
靶向治療
有學者通過對瘤細胞中表達血管內皮生長因子和環氧化酶-2的6例GC患者研究後提出,腫瘤生長均伴隨毛細血管增生,抗血管增生 靶向治療可以通過抑製腫瘤血管增生而抑製腫瘤生長;Cunha等則發現特定小RNA雙鏈複合物可以幹擾鉀離子通道蛋白EAG1,從而增 強IFN-γ對瘤細胞的殺傷作用;通過對惡性膠質瘤進行研究,Roth等發現整合素抑製物可以抑製血管增生及瘤細胞轉移;最近,Jin等對分子靶向藥物的研究表明,選擇性分子抑製劑MRK003和MK2206可以明顯抑製瘤細胞的生長、遷移。未來,分子靶向藥物研究的 進展必將為GC的治療打開一片新天地。
預後
盡管有多種治療措施,但患者預後仍較差。研究表明,一些基因的突變、重組及腫瘤標誌物的表達水平對該病預後有重要指導價值;Karnofsky評分、TP-53及異檸檬酸脫氫酶-1(isocitrate dehydrogenase 1,IDH1)基因以及Ki-67也與該病預後顯著相關,a-絲聯蛋白和IDH1R132H突變蛋白對患者預後也有重要價值;Kwon等進一步對突變型IDH1研究發現,表達突變型IDH1的II型患者的總生 存期及無進展生存期明顯延長;還有學者對GC患者的基因組雜交比較發現,染色體13q和10q的缺失以及7q的增加是預後不良的重要因子;最近,Erpolat等提出,缺氧誘導因子-1α、碳酸酐酶-9和骨橋蛋白等缺氧性指標的聯合應用對惡性膠質瘤患者生存期的預 測亦有重要價值。
【總結及展望】
由於GC臨床症狀複雜多樣、預後差,因此當患者出現精神及性格改變、顱內壓升高等表現,MRI提示顱內彌漫性病變時應考慮GC的可能,必要時行立體定向活檢術。鑒於其生物學特性,目前主張早診斷、早治療,以提高患者生存質量和延長生存期。盡管隨著研究的深入,GC的確診率有所提高,治療效果有所改善,但是預後仍然不佳,而進一步研究該病的病因、發病機製以及新的治療途徑和方法是當今亟待解決的課題。