2022年4月7日,生物醫學預印本bioRxiv在線發表了來自法國裏昂大學、美國加利福尼亞大學洛杉磯分校、法國遺傳生殖與發展研究所、德國歐洲病毒生物信息學中心和法國生物信息學研究所聯合發表的研究性文章,指出已通過蝙蝠和靈長類動物中 SARS-CoV-2 相互作用蛋白的不同進化軌跡確定了 COVID-19 的重要宿主決定因素。相關文章請參考 doi: https://doi.org/10.1101/2022.04.07.48746。

先說重點
眾所周知,病毒與宿主在相互作用過程中是不斷進化的,在進化的過程中,許多的宿主蛋白與病毒蛋白發生了相互作用,這些相互作用蛋白被稱為病毒相互作用蛋白(virus interacting proteins,VIPs)。
於是,科研人員對334種SARS-CoV-2相互作用蛋白進行了高通量進化分析,以識別SARS-CoV適應性位點並揭示現代人類、靈長類動物和蝙蝠之間的功能差異,進一步揭示在這一互作進化過程中,過去是如何塑造現代病毒庫和人類的。
通過這一關係,科研人員進一步鑒定出了具有適應性進化特征的81種靈長類動物和38種蝙蝠VIPs。
緊接著,科研人員圍繞著以上物種之間的共同點描繪了一個以此共同點為核心的適應性相互作用組,以此顯示出不同進化軌跡中與不同宿主譜係相關的宿主特異性決定因素。
研究人員發現,靈長類動物特異性適應進入因子TMPRSS2的證據表明其在宿主體內的重要性並可依據此因子預測病毒-宿主分子交互界麵。此外,與人類嚴重COVID-19(GWAS)相關的FYCO1位點顯示出靈長類動物古代適應性的進化特征,突出了其在SARS-CoV-2複製或發病機製中的重要性以及與蝙蝠宿主差異性的關係。蝙蝠多功能蛋白RIPK1的適應性進化也預示了宿主決定性因素的相關性。
文獻解析
COVID-19大流行是由SARS-CoV-2引起的,這是一種從蝙蝠病毒庫溢出的新型冠狀病毒(目前證據表明)。盡管進行了許多臨床試驗和疫苗,但疾病流行的風險仍然巨大,而且SARS-CoV-2易感性和COVID-19的嚴重程度在宿主層麵的決定因素在很大程度上仍然未知。研究表明,在靈長類動物和蝙蝠基因組中通過比較功能遺傳分析檢測到的陽性選擇特征可以揭示發生在病毒-宿主界麵上的重要進化因素。在這裏,科研人員使用 DGINN(基因創新檢測),共鑒定了38種蝙蝠和81種靈長類動物蛋白質,並帶有陽性選擇標記。包括ACE2受體在內的17個基因在哺乳動物的兩個目中都呈現出適應性標記,這表明常見的病毒-宿主相互作用和過去流行的冠狀病毒在某種程度上塑造了宿主的基因組。

值得注意的是,參與炎症性RIPK1泛素化和磷酸化的殘基在蝙蝠而非靈長類動物中存在迅速進化現象,這表明蝙蝠的炎症調節作用與人類是存在差異的。此外,科研人員在靈長類動物中發現了具有典型病毒宿主軍備競賽標記的殘基,例如進入因子TMPRSS2或自噬適配器FYCO1,可能是藥物靶標的宿主特異性體內重要界麵。在靈長類動物中適應的FYCO1位點與嚴重的COVID-19相關,這支持了它們在發病機製和複製中的重要性這一觀點。總體而言,本次研究確定了蝙蝠和靈長類動物SARS-CoV-2感染所涉及的功能性適應,這對現代病毒易感性和嚴重性的遺傳決定因素具有重要啟發意義。
蝙蝠和靈長類動物中SARS-CoV-2 VIP進化史的特征
由於病原病毒和宿主參與了進化軍備競賽,過去的流行病導致VIP基因中積累了適應性特征。當非同義密碼子替換率超過同義密碼子替換率時,可以通過對一組蛋白質編碼直係同源物的正選擇分析來識別適應性進化。科研人員對靈長類動物和蝙蝠的VIP進行了比較係統發育,發現在人類細胞中SARS-CoV-2蛋白的質譜分析中,血管緊張素轉換酶2(ACE2)受體和跨膜蛋白酶絲氨酸2(TMPRSS2),兩者都是病毒所必需的進入細胞。
蝙蝠和靈長類動物進化過程中具有正選擇特征的SARS-CoV-2 VIP的鑒定和比較分析
科研人員在蝙蝠和靈長類動物基因的自然選擇中發現了類似正向選擇的趨勢。其他SARS-CoV-2體外或臨床研究也將這些陽性選擇的基因確定為 SARS-CoV-2 VIP,從而證實了它們作為 SARS-CoV-2 調節劑或相互作用蛋白的可能。此外,陽性選擇的VIP與細胞周期控製和中心體行為生物學通路密切相關,這表明細胞分裂的控製以及中心體調節的細胞極化對體內SARS冠狀病毒的發展很重要。因此,這些VIP中的陽性選擇標記可能代表了宿主蛋白的適應性,即這些蛋白在與哺乳動物的數百萬年的共同進化中調節或與冠狀病毒相互作用,代表了一組進化上常見的冠狀病毒相互作用蛋白。
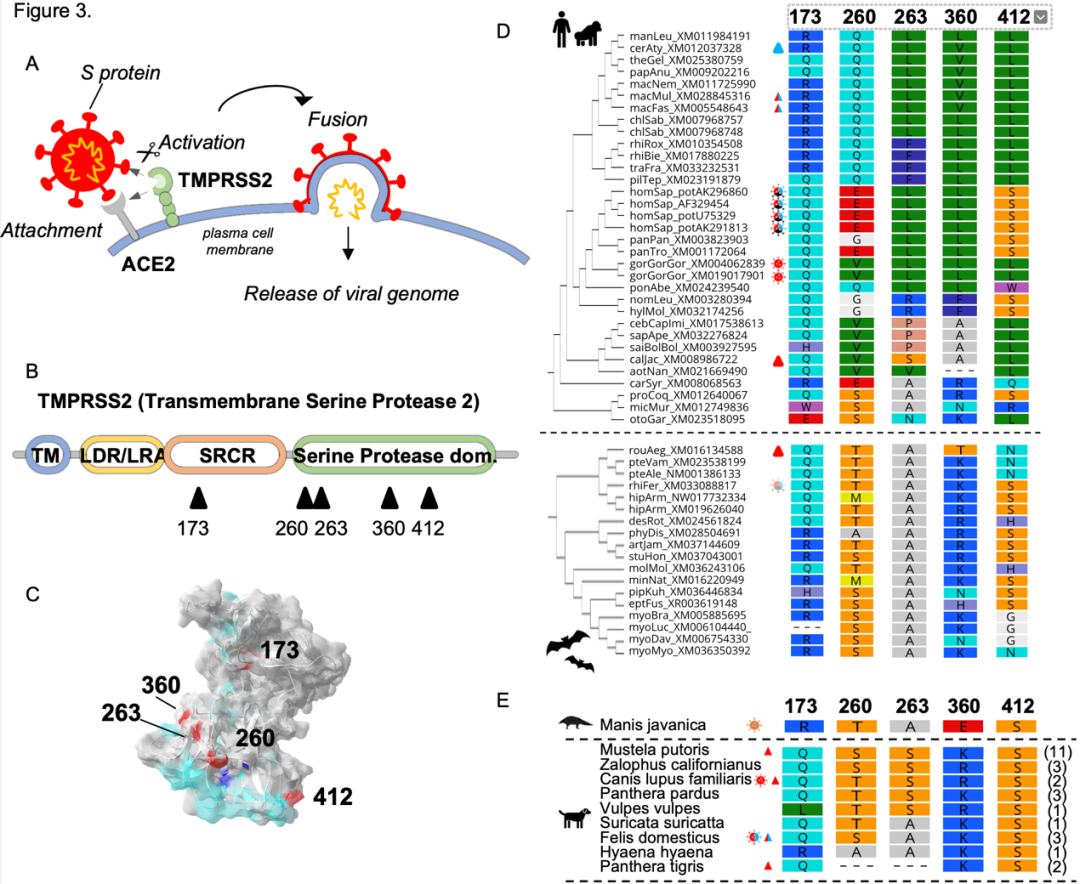
TMPRSS2中的SARS-CoV-2預測界麵在靈長類動物的適應性進化下進化,但在蝙蝠中沒有
在進化分析的指導下,科研人員對TMPRSS2進行誘變研究,以確定和SARS-CoV相關的決定因素,以及MPRSS2種間變異的功能含義。結果表明,TMPRSS2 中的正選擇特征與靈長類動物進化過程中SARS-CoV驅動的選擇壓力密切相關。而以上現象未在蝙蝠中發現。
FYCO1在靈長類動物進化過程中不同時間尺度參與SARS冠狀病毒發病機製或複製的證據
FYCO1參與微管運輸和自噬。然而,FYCO1是人類全基因組關聯研究(GWAS)中發現的極少數與嚴重COVID-19顯著相關的基因之一。表明FYCO1在SARS冠狀病毒發病機製或靈長類動物複製中的重要性。
RIPK1對人類調控至關重要的殘基處一直在蝙蝠中進行適應性進化
人RIPK1是一種銜接蛋白,通過腫瘤壞死因子α受體1(TNFR1)和Toll樣受體3和4 (TLR3/4)參與炎症,導致促生存、凋亡或壞死性凋亡信號。對RIPK1相互作用子的精心分析表明,它是參與關鍵炎症和細胞存活/死亡過程的79個細胞夥伴的中心樞紐。RIPK1與SARS-CoV-2 NSP12(RdRp)相互作用,並進一步參與多種細菌和病毒感染。
總結
分析SARS-CoV-2 VIP編碼序列的研究的核心是識別多個SARS-CoV-2相互作用蛋白位點,這可能反映了病毒和抗病毒分子軍備競賽的確切位點。因此,這些位點對SARS-CoV-2宿主決定性因素至關重要。此外,VIPs代表了重要的宿主-病原體交互界麵。因此,開發針對具有強烈病毒宿主軍備競賽標誌的抗藥物可能是一種有效的廣泛抗病毒策略。
原始出處:
Marie Cariou, Léa Picard, Laurent Guéguen, et al.Distinct evolutionary trajectories of SARS-CoV-2 interacting proteins in bats and primates identify important host determinants of COVID-19. bioRxiv, 2022.