本次ASCO大會上,斯坦福大學醫學院的Heather A. Wakeleeb報告了KEYNOTE-671研究的IA1中期分析結果,該重磅研究也已同步刊登於《新英格蘭醫學雜誌》。
KEYNOTE-671是一項評估帕博利珠單抗作為非小細胞肺癌(NSCLC)新輔助/輔助治療方案的療效的隨機、雙盲、III期臨床試驗(NCT03425643)。這項研究顯示,在25.2個月的中位隨訪時間中,帕博利珠單抗組的24個月無事件生存率(EFS)為62.4%,安慰劑組的這一數據為40.6%。這表明,與安慰劑組相比,帕博利珠單抗治療早期肺癌患者疾病進展、複發或死亡風險下降42%(HR 0.58;P<0.001)。
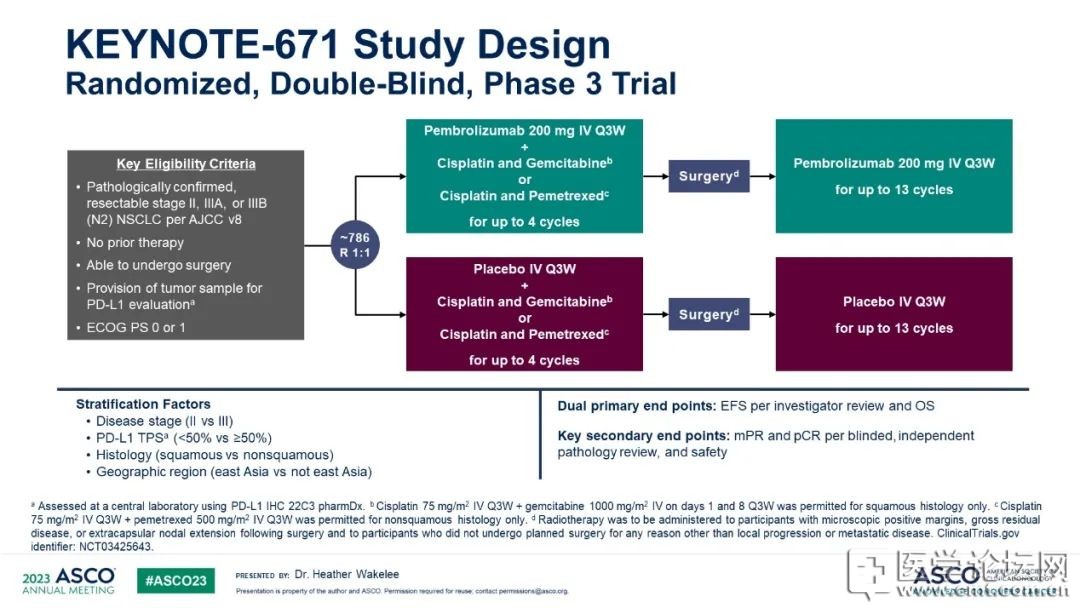
圖. KEYNOTE-671研究IA1分析結果發布
此前,帕博利珠單抗已顯示出其單藥及輔助治療在早期NSCLC中的療效,並且已經聯合化療用於轉移性疾病,該項研究在術前鉑類化療基礎上添加帕博利珠單抗/安慰劑作為新輔助治療,術後采用帕博利珠單抗/安慰劑作為的輔助治療,分析了圍術期全程免疫治療對NSCLC的療效。
KEYNOTE-671研究共納入了
797名患者II期、IIIA期或IIIB期(N
2期)可切除性NSCLC患者按照1:1被隨機分配至帕博利珠單抗組(397)或安慰劑組(400)。
入組患者術前在順鉑+吉西他濱/培美曲塞化療的基礎上,接受4個療程的帕博利珠單抗(200mg)/安慰劑(均為3周1次),在距第1療程開始的20周內接受手術。
術後4周進行13個療程的輔助治療:
帕博利珠單抗(200mg)/安慰劑(均為3周1次)。
截至2022年7月29日,中位隨訪時間為25.2個月。
亞組分析分層因素:
分期(II期vs.III期)、PD-L1 TPS(<50% vs.≥50%)、組織學(鱗狀細胞vs.非鱗狀細胞)和地區(東亞vs.非東亞)
。2個主要終點:EFS和總生存期(OS);3個次要終點:mPR(切除組織中腫瘤細胞≤10%)、pCR(ypT0/Tis ypN0)和安全性。
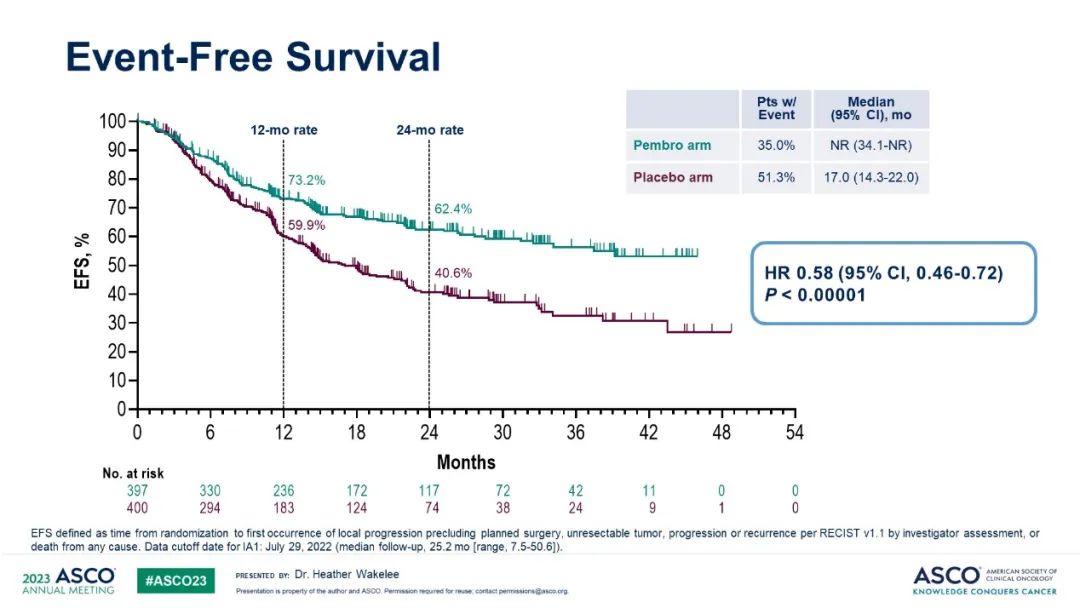
相比使用安慰劑,圍術期全程應用帕博利珠單抗顯著改善無事件生存率EFS,患者疾病複發、進展或死亡風險降低了42%(HR 0.58,P<0.00001),事件發生率35.0% vs.51.3%。
目前帕博利珠單抗組未達到中位EFS,安慰劑組中位EFS為17個月(95% CI,14.3-22),2年EFS別為62.4%和40.6%。
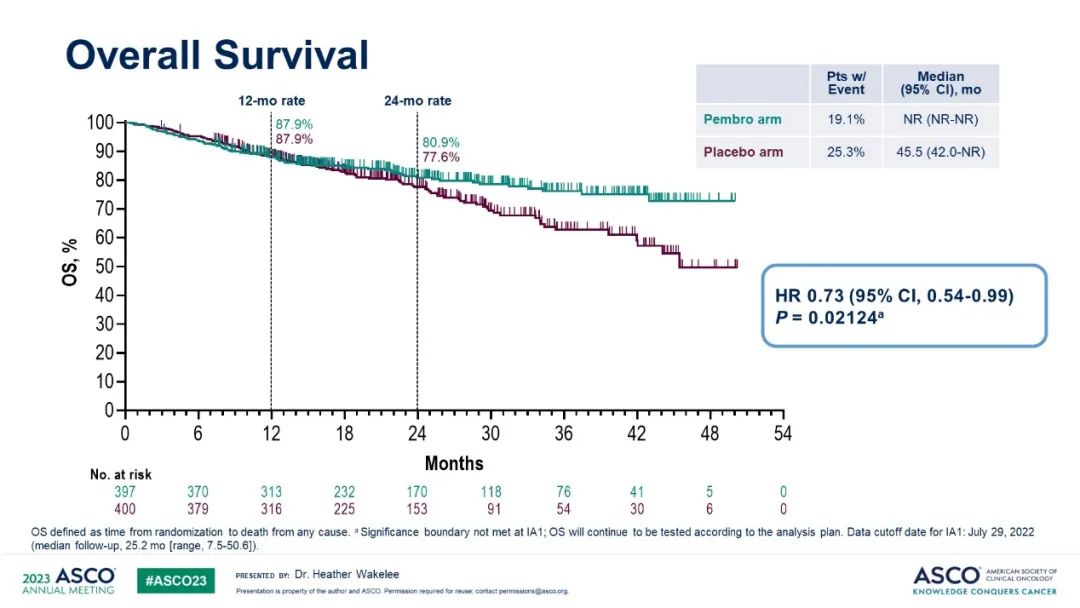
由於目前僅發生了177個事件,OS未達統計學終點,但兩組已出現分離趨勢,後續將繼續跟進隨訪數據(事件發生率19.1% vs.25.3%,HR 0.73,P=0.02124)。
帕博利珠單抗組有80.6%的患者接受了手術(R0切除:92%),安慰劑組接受手術比例為75.5%(R0切除:84%)。
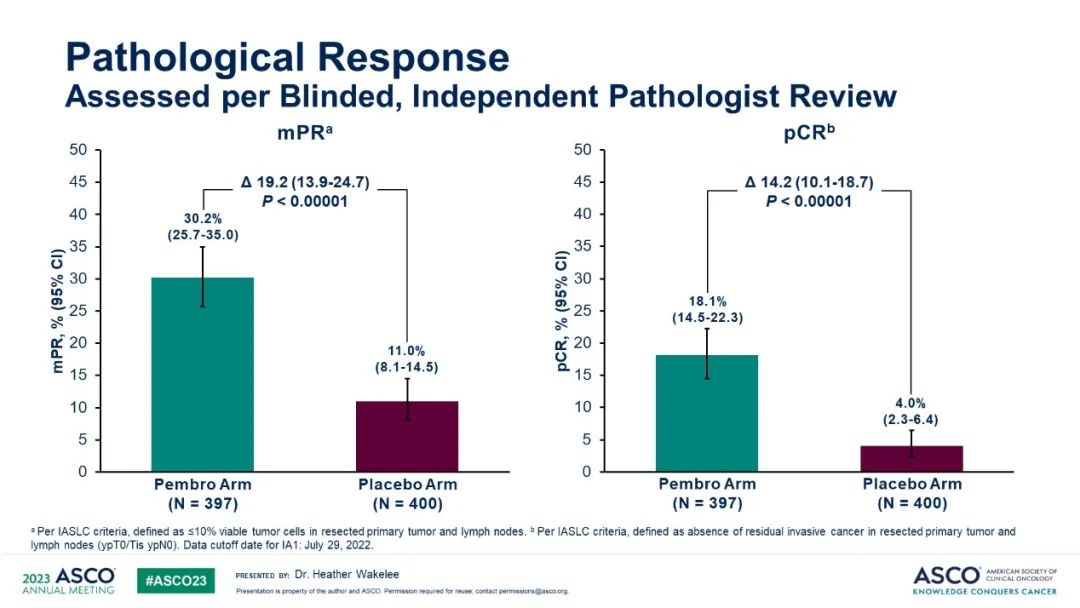
帕博利珠單抗組和安慰劑組的mPR率為30.2%和11%(人數120vs.44,差異19.2%,P<0.00001),pCR率為18.1%和4%(人數72vs.16,差異14.2%,P<0.00001)。
圖. KEYNOTE-671研究主要病理學緩解數據
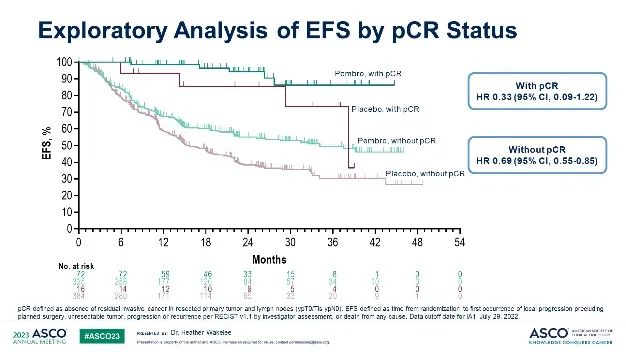
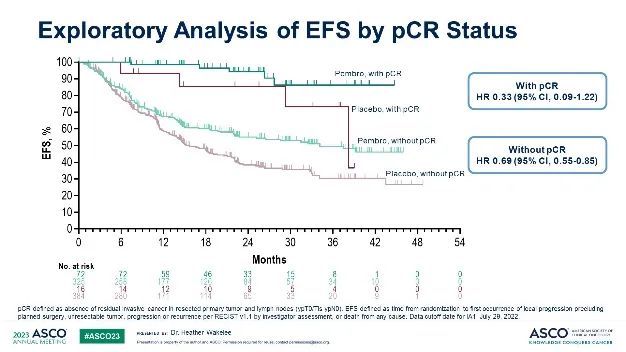
無論患者是否達到mPR或pCR,圍術期全程的帕博利珠單抗治療都會顯著提高EFS。
圖. KEYNOTE-671研究中pCR、mPR亞組的EFS
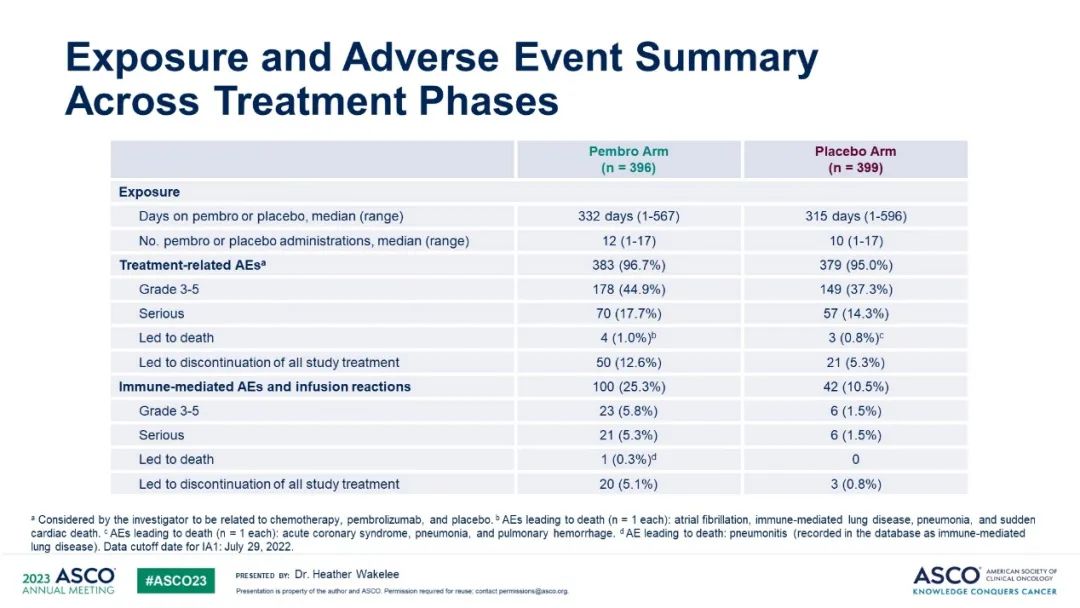
帕博利珠單抗組中44.9%的患者發生了治療相關的≥3級不良事件,安慰劑組發生率為37.3%。
治療相關不良事件導致治療終止發生率分別為12.6%和5.3%,導致死亡的比例分別為1%和0.8%;
免疫相關不良事件發生率分別為25.3%和10.5%。
最常見的≥3級不良事件:中性粒細胞計數減少、貧血、白細胞計數減少和血小板計數減少。
總體安全性可控。
無論PD-L1表達、病理學類型和腫瘤分期呈現如何結果,帕博利珠單抗±化療方案均可顯著改善EFS。
總之,該項III期研究發現,對於早期可切除的II期、IIIA期和IIIB期(N2期)NSCLC患者,術前帕博利珠單抗+化療+術後輔助帕博利珠單抗在EFS、pCR和mPR方麵提供了具有統計學意義和臨床意義的改善,而在OS方麵仍需進一步隨訪分析,且帕博利珠單抗的安全性與預期相符。
該項研究也暗示,在新輔助免疫治療後使用輔助免疫治療的圍術期全程免疫治療有望進一步提升治療效果。
針對非小細胞肺癌,免疫治療的最佳應用是術前新輔助治療,還是術後輔助治療,抑或是本研究中圍術期全程的爭論一直存在,本次ASCO大會上,來自哈佛醫學院的Mark M. Awad教授也帶來了他的見解。
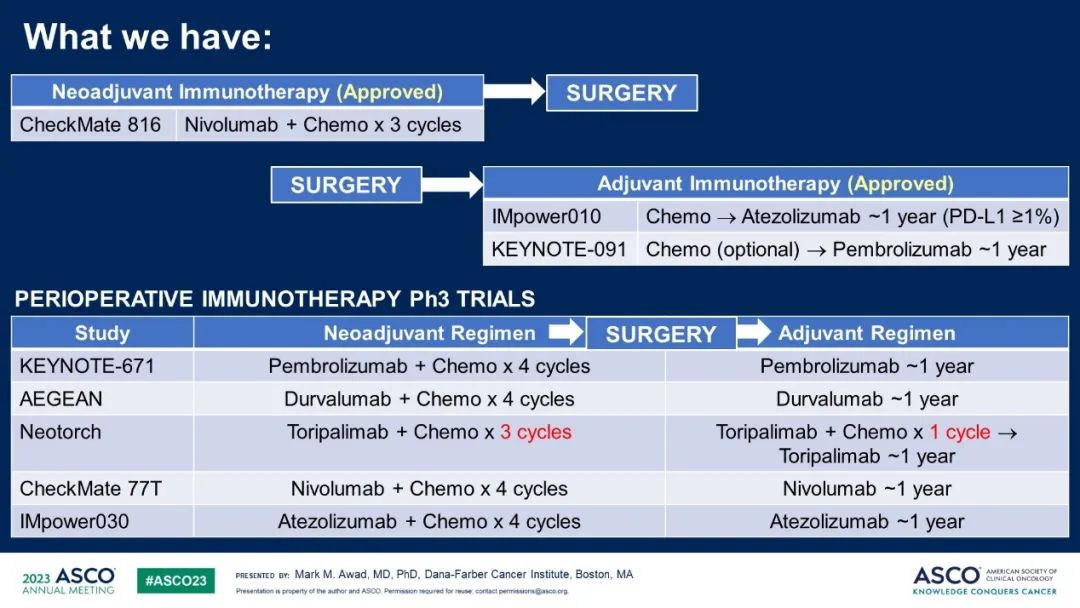
近年來PD-(L)1抑製劑迅速發展,2021年至今,阿替利珠單抗輔助治療(Impower010)、納武利尤單抗+化療新輔助治療(Checkmate-816)、帕博利珠單抗輔助治療(KeyNote-091)相繼獲批。過去兩個月開啟了圍術期免疫治療NSCLC的III期臨床試驗(AEGEAN and Neotorch),上述KeyNote-671的中期分析也帶來了充滿希望的結果。
但是免疫治療用於NSCLC仍存在許多疑問,Mark M. Awad教授針對以下幾個方麵進行了報告。
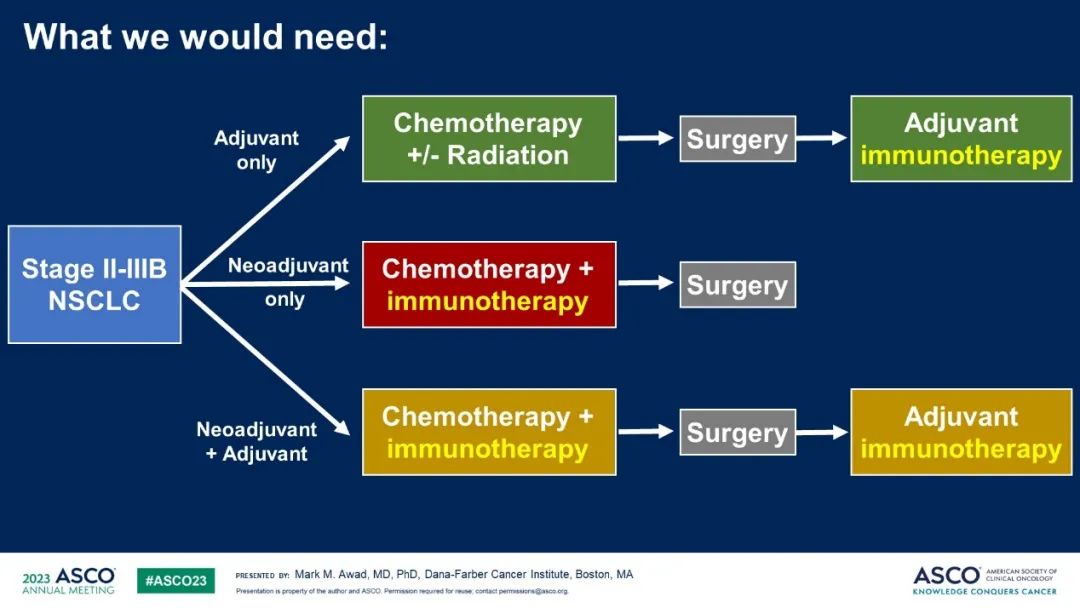
目前的臨床研究包括了術前新輔助化療(CheckMate-816)、術後輔助化療(Impower010,KeyNote-091)、圍術期全程免疫治療(KeyNote-671,AEGEAN,Neotorch,CheckMate-77T,Impower030)三個方麵,Mark M. Awad教授分析了這些研究的OS改善情況。
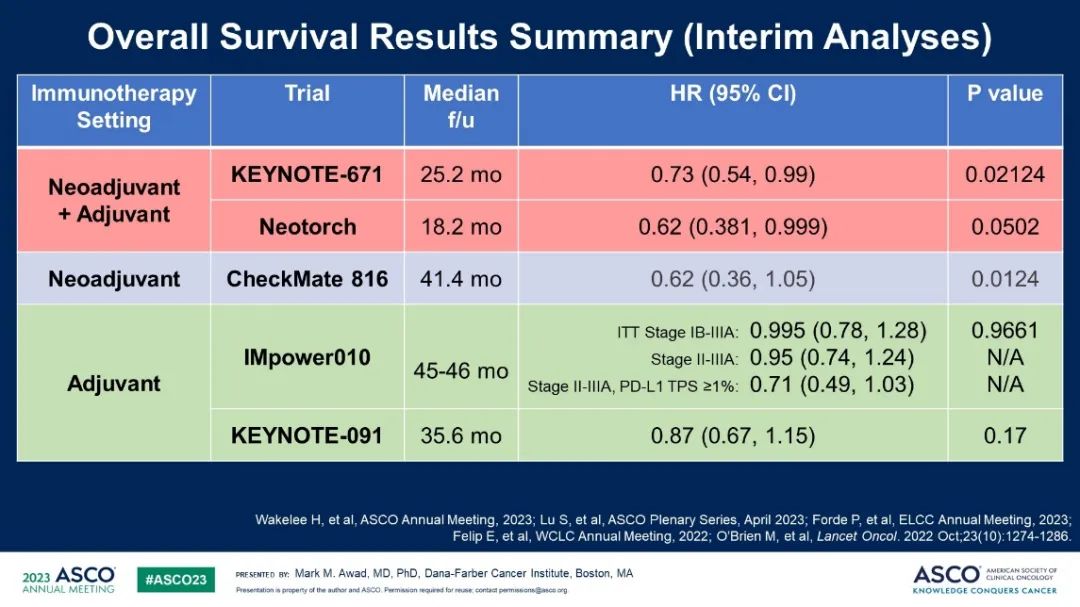
術後免疫輔助治療vs.安慰劑:中期分析未出現明顯OS差異(Impower010,KeyNote-091);
術前免疫新輔助治療vs.安慰劑:3年的(Checkmate-816)中期分析顯示,術前新輔助治療得到明顯OS獲益,但未達統計學終點,需跟進研究。(HR=0.62, P=0.0124);
圍術期免疫治療vs.安慰劑:KeyNote-671,Neotorch兩項研究均顯示差別,但未達統計學終點。
目前各項研究的中期結果分析顯示,免疫新輔助治療±輔助治療在OS受益方麵顯示出良好的前景。
免疫新輔助治療是否妨礙患者實施手術呢?幾項研究中,均有15-25%的患者未進行手術,但各項研究納入的患者基線特征差異較大,無法進行進一步的分析。
鑒於現有研究的隨機基線特征,很難判斷術後繼續免疫輔助治療是否能使患者受益。
需要更長的隨訪時間,幫助判斷EFS差異。
術後免疫治療可否省略:
NADIM-II研究中,盡管術後僅采用6個月的納武利尤單抗輔助治療, 相比術後觀察組,仍有顯著的PFS獲益,盡管術前治療策略並不一致,但仍然可以認為,在得到患者同意的情況下,術後有理由繼續實施免疫輔助治療。
對於突變患者的最優治療,現有研究樣本較小、結論矛盾,無明確定論。術後選擇采用免疫治療還是針對突變的靶向藥如奧希替尼仍然難以決策。
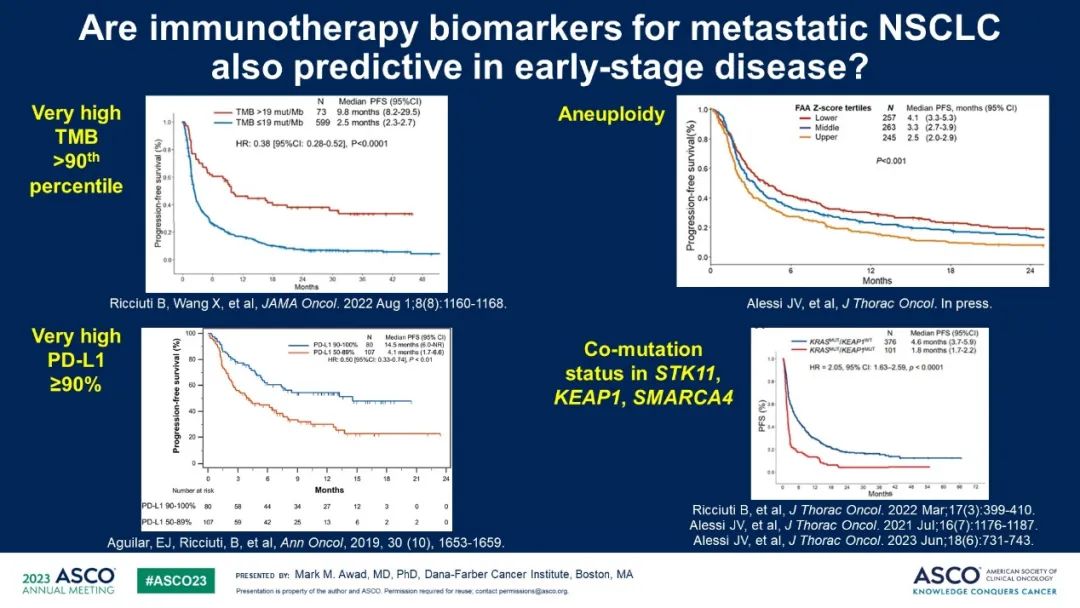
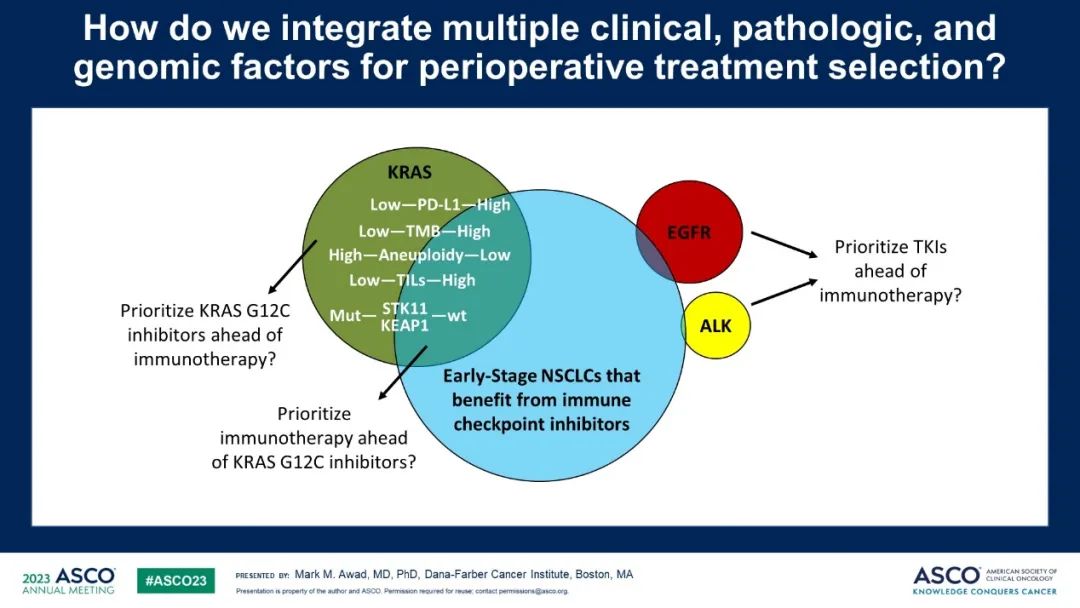
現有研究提示了高PD-L1、高TMB、低非整倍體率、野生型STK11+KEAP1+SMARCA4與更好的NSCLC免疫治療效果相關,那麼這些免疫治療生物標誌可否推廣於早期疾病的治療策略呢?據此講者提出了根據患者疾病臨床、病理、遺傳因素整合治療的建議。
對於少量EGFR/ALK突變的早期NSCLC,是否傾向於優先使用TKIs?
對於KRAS突變的早期NSCLC,是否根據不同突變對於免疫治療的獲益程度優先選擇相應療法?例如:高PD-L1、高TMB、低非整倍體率、高TILs、野生型STK11+KEAP1+SMARCA的早期NSCLC優先免疫治療,反之則有限KRAS G12C抑製劑治療。
[1]Wakelee H, Liberman M, Kato T, et al. Perioperative Pembrolizumab for Early-Stage Non-Small-Cell Lung Cancer [published online ahead of print, 2023 Jun 3].N Engl J Med. 2023;10.1056/NEJMoa2302983. doi:10.1056/NEJMoa2302983